Med Quality
Rejestracja wyrobów medycznych na Ukrainie
Wiodąca firma doradcza w zakresie rejestracji wyrobów medycznych i suplementów diety na Ukrainie oraz w Europie.
O nas
Med Quality
Qualitas Alta, Qualitas Melior, Qualitas Optima
Ukraińska firma, która świadczy usługi w zakresie rejestracji i certyfikacji wyrobów medycznych oraz suplementów diety, a także pomaga wejść na rynek Ukrainy i Europy z zachowaniem wszystkich wymogów regulacyjnych. Zapewniamy wdrożenie systemu jakości zgodnie ze standardami ISO 13485 i 22000 oraz dołożymy wszelkich starań, aby Państwa produkty jak najszybciej trafiły na rynek. Twórzmy razem rynek wysokiej jakości produktów!
Nasze usługi
Pełne wsparcie w procesie certyfikacji w jednostce oceny zgodności dla wyrobów medycznych lub przeprowadzenie procedury samodeklaracji poprzez wpis do Rejestru Państwowej Służby Leków.
Komunikacja z producentem, analiza dokumentów, tłumaczenie, składanie dokumentów do jednostki oceny zgodności oraz współpraca z Państwową Służbą Leków.
Świadczenie usług upoważnionego przedstawiciela na terytorium Ukrainy.
Zapewnienie pełnego przedstawicielstwa z systemem obsługi skarg konsumentów oraz wsparciem w budowie systemu nadzoru po wprowadzeniu do obrotu wyrobów medycznych.
Zapewnienie szybkiego przygotowania dokumentacji dla sprawnego wejścia na rynek.
Wdrożenie systemu jakości zgodnie ze standardem ISO 13485 gwarantuje Państwa firmie zgodność z najwyższymi standardami w zakresie wyrobów medycznych oraz znacząco podnosi konkurencyjność podczas udziału w zamówieniach publicznych.
Wsparcie we wdrażaniu skutecznego systemu zarządzania jakością, który zapewnia zgodność produktów oraz spełnienie obowiązujących wymogów dla skutecznego wprowadzania wyrobów medycznych na rynek.
Pełny cykl opracowania dokumentacji technicznej wyrobów medycznych: od analizy ryzyka po wsparcie w organizacji i realizacji niezbędnych badań.
Gwarancja zgodności z obowiązującymi wymogami regulacyjnymi oraz stałe wsparcie na wszystkich etapach przygotowania wyrobu medycznego do wprowadzenia na rynek.
Określenie możliwych ścieżek wejścia wyrobów medycznych na rynek europejski.
Analiza dokumentacji, budowa systemu jakości, opracowanie i aktualizacja dokumentacji technicznej zgodnie z wymaganiami rozporządzeń MDR 2017/745 oraz IVDR 2017/746.
Planowanie wejścia na rynek z jasno określonymi i przejrzystymi etapami.
Wsparcie w wyborze jednostki notyfikowanej na terenie UE.
Określenie wykazu obowiązujących wymagań oraz opracowanie dokumentacji niezbędnej do produkcji suplementów diety.
Tłumaczenie i korekta oznakowania oraz instrukcji dla suplementu diety.
Weryfikacja danych naukowych dotyczących skuteczności suplementu oraz twierdzeń umieszczanych w instrukcji i wykorzystywanych w działaniach marketingowych.
Organizacja i prowadzenie szkoleń dotyczących rejestracji i certyfikacji wyrobów medycznych, standardów ISO 13485, ISO 22000 oraz innych specyficznych zastosowalnych norm dla wyrobów medycznych lub suplementów diety.
Organizacja i realizacja indywidualnych kursów, podczas których każdy uczestnik otrzymuje nie tylko wiedzę teoretyczną, ale także praktyczne umiejętności niezbędne do efektywnej pracy w sektorze wyrobów medycznych i suplementów diety.
Dlaczego wybierają nas?

Zespół
Nasi specjaliści posiadają wieloletnie doświadczenie i wiedzę niezbędną do skutecznej rejestracji wyrobów medycznych i suplementów diety.

Indywidualne podejście
Uwzględniamy wyjątkowość każdego produktu i zapewniamy pełne wsparcie na wszystkich etapach rejestracji.

Energia i orientacja na rezultat
Jesteśmy szczerze oddani swojej pracy i zaangażowani w osiągnięcie sukcesu przez naszych klientów.

Niezawodność
Dotrzymujemy naszych zobowiązań, realizujemy ustalenia rzetelnie i na czas.
Nasi klienci















Aktualności
Przeprowadzono webinar na temat analizy ryzyka wyrobów medycznych zgodnie z wymaganiami ISO 13485 i ISO 14971.
Dyrektor Med Quality 2 kwietnia 2025 roku przeprowadził szkolenie dotyczące wymagań standardu ISO 13485:2016.
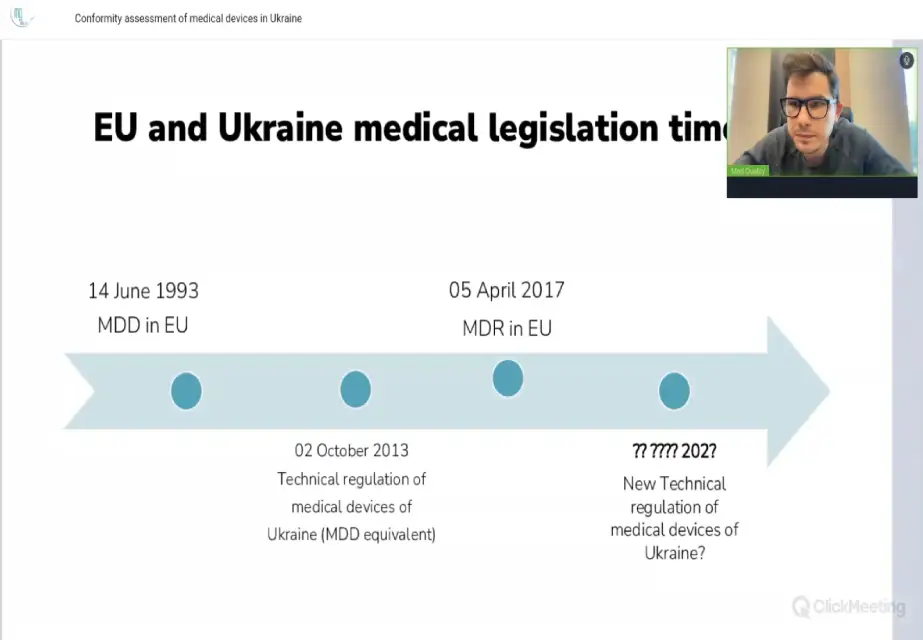
Dyrektor Med Quality Władysław Kasjanenko przeprowadził webinar na temat „Ocena zgodności wyrobów medycznych w Ukrainie”.
Webinaria

Ocena zgodności indywidualnych wyrobów medycznych (custom-made): co jest naprawdę wymagane, a co zbędne?
26.05.2026

Druk 3D w wyrobach medycznych: certyfikacja, wymagania regulacyjne i rzeczywiste ryzyka
23.06.2026

Certyfikacja komponentów wyrobów rehabilitacyjnych: kiedy stają się wyrobem medycznym i jak je prawidłowo sklasyfikować? Wykorzystanie druku 3D w produkcji
21.07.2026

Oznakowanie wyrobów medycznych. Wymagania Rozporządzenia Technicznego nr 753 oraz normy ISO 15223-1. Jak uniknąć kar?
28.08.2026

ISO 13485:2016 dla producentów wyrobów rehabilitacyjnych oraz innych wyrobów medycznych wykonywanych na zamówienie: co zrobić z systemem zarządzania jakością?
22.09.2026

Organizacja i przeprowadzanie badań przedklinicznych protez, ortez oraz innych wyrobów rehabilitacyjnych: od badań wytrzymałościowych po biokompatybilność
06.10.2026

Nadzór po wprowadzeniu do obrotu (PMS): jak producentowi nie „ponieść porażki” po wprowadzeniu wyrobu medycznego na rynek
20.10.2026

Certyfikacja implantów: od stomatologii do osteointegracji, jak prawidłowo przeprowadzić ocenę zgodności?
24.11.2026

Nadzór rynkowy 2027: jak przygotować się i przejść kontrolę bez kar finansowych
22.12.2026