Med Quality
Реєстрація медичних виробів в Україні
Qualitas Alta, Qualitas Melior, Qualitas Optima
провідна компанія консультативних послуг по реєстрації медичних виробів та дієтичних добавок в Україні та Європі.
Про нас
Med Quality
Qualitas Alta, Qualitas Melior, Qualitas Optima
Українська компанія, яка надає послуги з реєстрації та сертифікації медичних виробів та дієтичних добавок та допомагає вийти на ринок України та Європи з дотримання усіх регуляторних вимог. Ми забезпечуємо впровадження системи якості за стандартами ISO 13485 та 22000 та докладемо максимум зусиль щоб ваша продукція якомога швидше вийшла на ринок. Давайте формувати ринок якісної продукції разом!
Наші послуги
Повний супровід у процесі сертифікації в органі з оцінки відповідності щодо медичних виробів або проведення процедури самодекларування через внесення в Реєстр Держлікслужби. Ведення комунікації з виробником, аналіз документів, переклад, подача документів в орган з оцінки відповідності та взаємодія з Держлікслужбою.
Надання послуг уповноваженого представника на території України. Забезпечення повного представництва з системою обробки скарг споживачів та допомогою у побудові системи пост-маркетингу за випущеними на ринок медичними виробами. Забезпечення швидкого оформлення для оперативного виходу на ринок.
Впровадження системи якості за стандартом ISO 13485 гарантує вашій компанії відповідність найвищим стандартам у сфері медичних виробів та значно підвищує рейтинг під часть участі у державних закупівлях. Допомога у налаштуванні ефективної системи управління якістю, що забезпечує відповідність продукції та дотримання застосовних вимог для успішної реалізації медичних виробів на ринку.
Повний цикл розробки технічної документації для медичних виробів: від аналізу ризиків до допомоги у організації та проведенні необхідних випробувань. Гарантія відповідності застосовним регуляторним вимогам та постійна підтримка на всіх етапах підготовки медичного виробу до виходу на ринок.
Визначення можливих шляхів виходу медичних виробів на Європейський ринок. Аналіз документів, побудова системи якості, розробка та актуалізація технічної документації щоб відповідати вимогам Регулювання MDR 2017/745 та IVDR 2017/746. Планування виходу на ринок з чіткими та прозорими етапами. Допомога у виборі нотифікованого органу на території ЄС.
Визначення переліку застосованих вимог, розробка документів для здійснення виробництва дієтичних добавок. Переклад та вичитка маркування та інтрукцій на дієтичну добавку. Перевірка наукових даних щодо ефективності дієтичної добавки та тверджень, які вносяться в інструкцію та які використовуватимуться у маркетинговій діяльності.
Організація та проведення навчання щодо реєстрації та сертифікації медичних виробів, стандартам ISO 13485, ISO 22000 та іншим специфічним застосовним стандартам щодо медичних виробів або дієтичних добавок. Організація та проведення індивідуальних курсів, де кожен учасник отримує не тільки теоретичні знання, а й практичні навички, необхідні для успішної роботи у сфері медичних виробів та дієтичних добавок.
Чому обирають нас?

Команда
наші фахівці мають багаторічний досвід і знання, необхідні для успішної реєстрації медичних виробів та дієтичних добавок.

Індивідуальний підхід
враховуємо унікальність кожного продукту і забезпечуємо повну підтримку на всіх етапах реєстрації.

Енергійність та націленість на результат
ми щиро віддані своїй справі, та зацікавлені у досягненні нашими клієнтами успіху.

Надійність
ми дотримуємося своїх зобов’язань, реалізуємо домовленості якісно та вчасно.
Наші клієнти















Новини
Директор Med Quality 2 квітня 2025 року провів навчання щодо вимог стандарту ISO 13485:2016
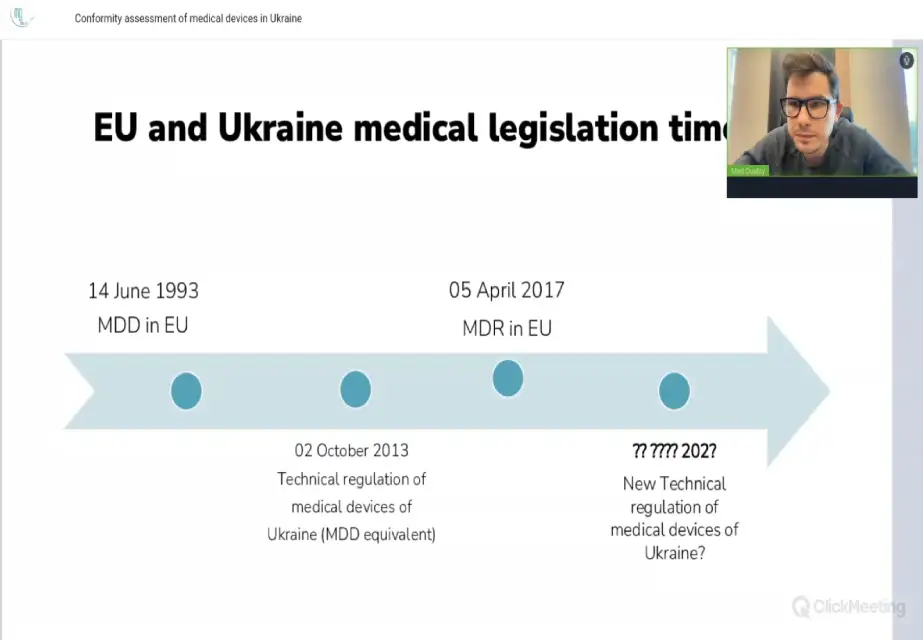
Директор Med Quality Владислав Касьяненко провів вебінар на тему «Оцінка відповідності медичних виробів в Україні»
Нещодавно компанія Med Quality провела вебінар на тему: "Як вийти на європейський ринок українському виробнику медичних виробів? Практичні поради"
Вебінари

3D-друк у медичних виробах: сертифікація, регуляторні вимоги та реальні ризики
23.06.2026

Сертифікація комплектуючих засобів реабілітації: коли вони стають медичним виробом і як їх правильно оформити? Використання 3Д-друку у виробництві
21.07.2026

Маркування медичних виробів. Вимоги Технічного регламенту № 753 та стандарту ISO15223-1. Як уникнути штрафів?
28.08.2026

ISO 13485:2016 для виробників засобів реабілітації та інших медичних виробів, виготовлених на за: що робити з системою якості?
22.09.2026

Організація та проведення докілінічнихвипробувань протезів, ортезів та інших засобів реабілітації: від випробування на міцність до біосумісності
06.10.2026

Постмаркетинговий нагляд (PMS): як виробнику не “провалитись” після виходу медичного виробу на ринок
20.10.2026

Сертифікація імплантів: від стоматології до остеоінтеграції, як правильно провести оцінку відповідності?
24.11.2026